В этом году лауреатами Нобелевской премии по физиологии и медицине стали биохимик Каталин Карико (Katalin Karikó) и иммунолог Дрю Вайсман (Drew Weissman) за «открытия, касающиеся модификаций нуклеозидных оснований, которые позволили разработать эффективные мРНК-вакцины против COVID-19» («for their discoveries concerning nucleoside base modifications that enabled the development of effective mRNA vaccines against COVID-19»).
В ходе совместной работы на рубеже тысячелетий Карико и Вайсман совершили открытие, позволившее применять в медицине матричные РНК (мРНК), полученные путем транскрипции in vitro. Поскольку мРНК служат матрицами для синтеза белка в ходе трансляции, с их помощью можно заставить клетки-мишени синтезировать нужные белки. До исследований Карико и Вайсмана самым серьезным препятствием на пути внедрения препаратов на базе мРНК в клиническую практику было вызываемое ими воспаление и низкая эффективность трансляции. Карико и Вайсман показали, что введение определенных химических модификаций в нуклеотиды в составе синтезированных in vitro мРНК предотвращает нежелательную воспалительную реакцию и повышает эффективность трансляции. Совместная деятельность двух ученых дала толчок к разработке препаратов на основе синтезированных in vitro мРНК. Первым таким средством, поступившим на службу человечеству, стала вакцина против SARS-CoV-2, выпущенная в течение года после начала пандемии.
Матричные РНК (мРНК) синтезируются в клеточном ядре на основе ДНК в ходе транскрипции. Молекула мРНК — это «сообщение» об аминокислотной последовательности одного белка, передаваемое из ядра в цитоплазму, где оно прочитывается аппаратом синтеза белка в ходе трансляции (по-английски эта молекула называется messenger RNA — «РНК-посланник»). Этот тип молекул был открыт в 1961 году группой французских ученых, через четыре года получивших за эти исследования Нобелевскую премию. В 1962 году было показано, что при добавлении изолированной из печени мРНК в культуру клеток на ее матрице синтезируется белок (M. Niu et al., 1962. Rna-induced biosynthesis of specific enzymes). В 1982 году ученые научились проводить транскрипцию мРНК в пробирке с помощью очищенных бактериальных и вирусных РНК-полимераз (K. Kruger et al., 1982. Self-splicing RNA: Autoexcision and autocyclization of the ribosomal RNA intervening sequence of tetrahymena). А в 1989 году был найден эффективный способ доставки мРНК в клетки путем ее смешивания с синтетическим липидом, молекулы которого окружали РНК, формируя оболочку (R. Malone et al., 1989. Cationic liposome-mediated RNA transfection).
Эти исследования открыли потенциал для использования мРНК в медицине, показав, что можно направлять в клетки организма генетическую информацию, которая будет ими прочитана и использована. Потенциальные медицинские направления использования мРНК — это иммунотерапия (вакцины против вирусов и борьба с раковыми клетками), замена белков, которые не функционируют из-за генетических заболеваний, и регенеративная медицина (доставка в поврежденные ткани мРНК факторов роста, стимулирующих восстановление) (Q. Duan et al., 2022. How far are the new wave of mRNA drugs from us? mRNA product current perspective and future development).
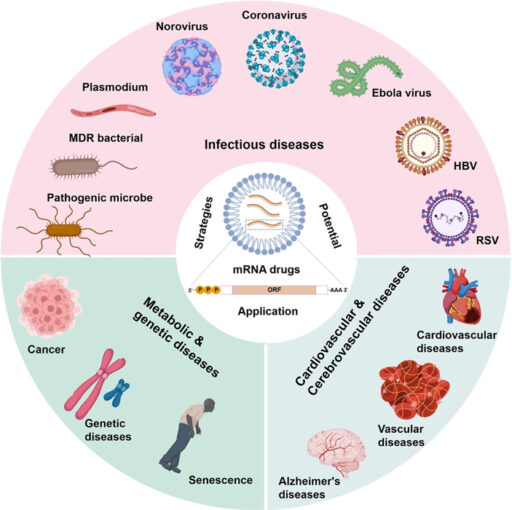
Ожидается, что терапия на основе мРНК станет эффективным средством для лечения многих заболеваний, включая инфекции, метаболические генетические заболевания, рак, сердечно-сосудистые и цереброваскулярные заболевания. Рисунок из статьи S. Qin et al., 2022. mRNA-based therapeutics: powerful and versatile tools to combat diseases
Но на пути к медицинскому применению мРНК еще оставались препятствия. Самое серьезное из них — нежелательная реакция врожденного иммунитета на попадание таких молекул в клетку. Врожденный иммунитет — первая линия защиты организма от патогенов, эволюционно древняя. Он активируется, когда так называемые Толл-подобные рецепторы (Toll-like receptors, TLR) узнают консервативные молекулярные признаки патогенов: например, рецептор TLR3 распознает двуцепочечную РНК — явный признак вирусной инфекции. Из-за активации врожденного иммунитета синтезированными in vitro мРНК они, вместо того чтобы служить матрицами для синтеза целевого белка, вызывают воспаление (R. Verbeke et al., 2022. Innate immune mechanisms of mRNA vaccines).
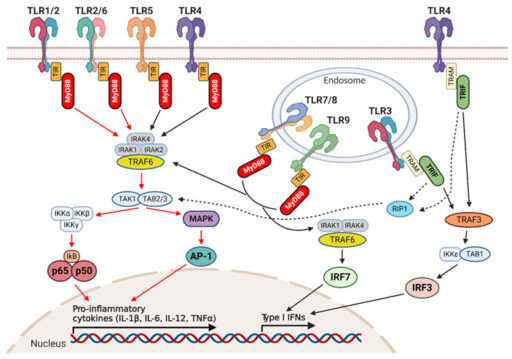
Толл-подобные рецепторы (TLR) клетки и сигнальные пути, которые они активируют. Одни типы TLR дежурят на внешней мембране клетки, другие смотрят внутрь эндосом — мембранных пузырьков, образующихся при поглощении клеткой чего-либо (например, вирусов). При связывании с лигандом TLR запускают каскад химических реакций, приводящий к активации в ядре генов, кодирующих интерфероны и провоспалительные факторы. Рисунок из статьи A. Di Lorenzo et al., 2020. Toll-Like Receptor 2 at the Crossroad between Cancer Cells, the Immune System, and the Microbiota
Здесь на сцене появляются новоиспеченные лауреаты.
Каталин Карико (Katalin Karikó) родилась 17 января 1955 года в небольшом венгерском городке Кишуйсаллаш. Она училась в Сегедском университете на биохимика и там же получила степень доктора. Проработав несколько лет на позиции исследователя в Институте биохимии (Сегед, Венгрия), она в 1985 году переехала в США. В 1989 году Карико устроилась в Пенсильванский университет на должность адъюнкт-профессора. Там она и выполнила исследования, отмеченные Нобелевским комитетом. Нужно отметить, что в процессе своей работы в университете Карико постоянно испытывала недостаток финансирования, несмотря на поддержку некоторых влиятельных коллег. Отчасти это было вызвано тем, что в 90-е годы тема мРНК на некоторое время выпала из научного мейнстрима и грантовые заявки по этой теме удовлетворялись менее охотно. Карико пришлось перейти в отделение нейрохирургии (Department of Neurosurgery), чтобы зарабатывать себе на жизнь, но она продолжала свои исследования. Карико так и не была повышена до полного профессора в Пенсильванском университете. В 2013 году она перешла в компанию BioNTech, заняв должность вице-президента компании, и там уже смогла применить весь свой опыт исследований мРНК.
Дрю Вайсман (Drew Weissman) родился 7 сентября 1959 года в Лексингтоне (Массачусетс, США). Он тоже учился на биохимика — в Брандейском университете, докторскую защитил по иммунологии и микробиологии в Бостонском университете в 1987 году. Затем работал в нескольких научных учреждениях в США, одно время — под руководством Энтони Фаучи. Вайсман перешел в Медицинскую школу имени Перельмана (Perelman School of Medicine) при Пенсильванском университете в 1997 году, где быстро присоединился к исследованиям, которые вела Карико.
Карико и Вайсман задались вопросом, почему РНК из одних источников — например, синтезированные in vitro или бактериальные — являются иммуногенными (то есть вызывают иммунный ответ), а из других — например, эукариотические мРНК, даже чужеродные — не вызывают. Исследователи показали, что иммуногенные РНК узнаются рецепторами TLR3, TLR7 и TLR8, работающими в эндосомах. Поступающие извне РНК захватываются клеткой путем эндоцитоза: клетка «обнимает» их частью своей мембраны, заключая в пузырек — эндосому. При этом активируются встроенные в эндосомальную мембрану рецепторы TLR, и, если им удается связаться с РНК, то запускается иммунный ответ.
Под руководством Карико и Вайсмана было установлено, что иммунитет не реагирует на эукариотические РНК благодаря тому, что нуклеотиды в их составе имеют особые химические модификации, не свойственные бактериальным РНК (K. Karikó et al., 2005. Suppression of RNA Recognition by Toll-like Receptors: The Impact of Nucleoside Modification and the Evolutionary Origin of RNA). Эти модификации происходят в клетках посттранскрипционно — после синтеза РНК — и служат для регуляции трансляции. Кроме того, как оказалось, благодаря этим модификациям клеточные TLR распознают инфекцию: если их нет в РНК — она точно чужеродная.
При синтезе мРНК in vitro в то время использовали только немодифицированные нуклеотиды, поэтому и получали сильный иммунный ответ: клетки распознавали молекулы как признак вторжения. Модификации, снижавшие иммунный ответ в эксперименте, — это добавление метильной группы или серы к определенным атомам углерода в молекулах нуклеотидов, а также превращение уридина в псевдоуридин. Хотя в клетке эти модификации производятся посттранскрипционно, команда Карико и Вайсмана при синтезе РНК in vitro добавляла в пробирку модифицированные нуклеотиды вместо стандартных или вместе с ними в различных соотношениях, меняя тем самым их долю в получающихся молекулах РНК. Оказалось, что способность молекулы РНК вызывать неспецифическую иммунную реакцию снижается пропорционально количеству модифицированных нуклеотидов в ее составе. Так и был найден оптимальный «рецепт» для приготовления неиммуногенных мРНК.
Позже та же команда показала, что замена уридина на псевдоуридин в составе синтезированных in vitro мРНК повышает эффективность синтеза белка (K. Karikó et al., 2008. Incorporation of Pseudouridine Into mRNA Yields Superior Nonimmunogenic Vector With Increased Translational Capacity and Biological Stability). Эффект достигается благодаря тому, что регуляторный фермент РНК-зависимая протеинкиназа (protein kinase R), подавляющий синтез белка путем инактивации одного из белков — факторов инициации трансляции, распознает уридин в составе мРНК, а псевдоуридин — не распознает (B. Anderson et al., 2010. Incorporation of pseudouridine into mRNA enhances translation by diminishing PKR activation).
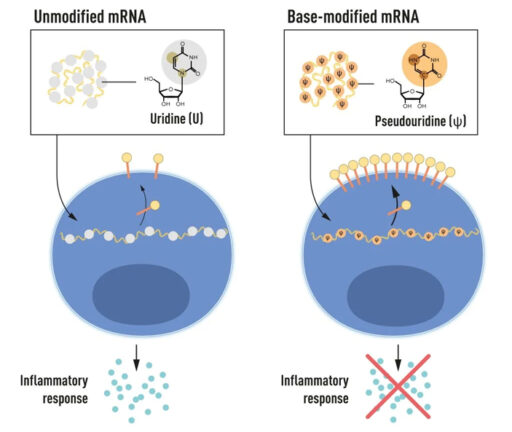
Краткая иллюстрация открытий лауреатов: замена уридина на псевдоуридин в синтезированной in vitro мРНК подавляет воспалительную реакцию и повышает продукцию белка. Рисунок с сайта nobelprize.org
Одно из возможных применений синтезированный in vitro мРНК в медицине — изготовление вакцин. Существующие типы вакцин основаны на использовании дезактивированных вирусных частиц или отдельных вирусных белков. Также используются векторные вакцины, где ген вирусного белка, на который после прививки должен реагировать иммунитет, вставлен в геном специального вируса-вектора, который доставляет его в клетку. Все эти технологии требуют использования клеточных культур и последующей очистки от компонентов клеток, что делает производство вакцин ресурсозатратным и медленным. Благодаря синтезу РНК in vitro возможно быстрое получение достаточного количества мРНК без примесей. При попадании в клетки организма специально подготовленная вакцинная мРНК служит матрицей для синтеза вирусного белка. Оставшись невостребованным клеткой, он обнаруживается специальными белками и режется на части — пептиды, которые выставляются на клеточной поверхности для демонстрации лимфоцитам.
Первая мРНК вакцина была выпущена на рынок в 2021 году. Она представляет собой мРНК S-белка вируса SARS-CoV-2, заключенную в липидную оболочку, и сейчас имеет торговое название Comirnaty.
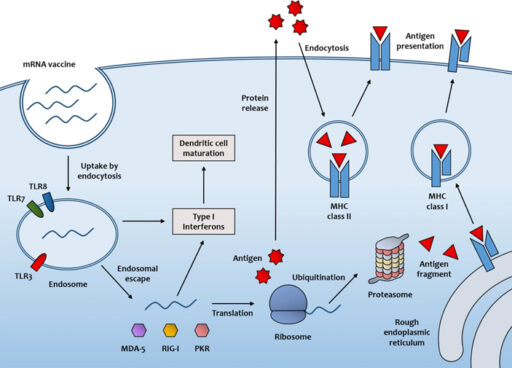
Принцип работы мРНК вакцины: мРНК, доставленная в цитоплазму клеток, напрямую использует клеточную систему трансляции для синтеза целевых белков. Эти белки далее попадают в протеасомы, где разрезаются на пептиды, которые перемещаются на клеточную мембрану с помощью белков главного комплекса гистосовместимости и узнаются Т-лимфоцитами. Рисунок из статьи S. Kwon et al., 2022. mRNA vaccines: the most recent clinical applications of synthetic mRNA
Успех применения мРНК в борьбе с COVID-19, безусловно, вдохновил ученых. Активно ведутся разработки мРНК-вакцин против других вирусов, в том числе — против вируса гриппа. Безусловно, Карико и Вайсман прошли важные вехи на пути к применению синтезированных in vitro мРНК в клинической практике, но важно помнить, что это достижение — заслуга многих тысяч людей.
Галина Клинк
ИСТОЧНИК: Элементы https://elementy.ru/novosti_nauki/434147/Nobelevskaya_premiya_po_fiziologii_i_meditsine_2023

