Но за последние несколько десятков лет продолжительность жизни увеличилась не так уж сильно, так как человечество исчерпало все простые методы увеличения срока жизни: гигиена, вакцины, антибиотики, здоровый образ жизни.
В некоторых странах продолжительность жизни даже уменьшилась, потому что люди начали питаться более дешевой калорийной пищей, что приводит к эпидемиям ожирения. Кроме того, увеличение срока жизни вовсе не гарантирует ее качество. Раньше люди умирали от инфекций в раннем возрасте. Теперь очень многие имеют шанс дожить до глубокой старости.

За последние 100 лет средняя продолжительность жизни человека в развитых странах выросла почти вдвое. На это есть объективные причины: уменьшение детской смертности, лечение большинства острых болезней, рост качества жизни, существенное снижение числа смертей по небиологическим причинам, таким как война.
Дело в том, что последние несколько десятков лет продолжительность жизни увеличилась не так уж сильно, так как человечество исчерпало все простые методы увеличения срока жизни: гигиена, вакцины, антибиотики, здоровый образ жизни. В некоторых странах продолжительность жизни даже уменьшилась, потому что люди начали питаться более дешевой калорийной пищей, что приводит к эпидемиям ожирения. Кроме того, увеличение срока жизни вовсе не гарантирует ее качество. Раньше люди умирали от инфекций в раннем возрасте. Теперь очень многие имеют шанс дожить до глубокой старости.
Но некоторые гены изменяют свою активность, не меняя первичной структуры, — эти изменения называются эпигенетическими. Например, к цитозину — одному из азотистых оснований ДНК — может присоединиться метильная группа, и это будет влиять на выработку того или иного белка в определенный момент времени. Это естественный процесс, благодаря которому клетки печени, например, имеют свой профиль активных генов по сравнению с нейронами головного мозга, несмотря на то что последовательность ДНК всех клеток тела одинаковая. Однако в ответ на стресс, воспаление, при укорочении или повреждении хромосом в процессе деления клеток эпигенетический профиль клетки может меняться, что приводит к возрастному изменению активности генов, в том числе жизненно важных.
Джордж Кристофер Уильямс — американский эволюционный биолог. Профессор биологии Государственного Университета Нью-Йорка.
В 1957 году эволюционный биолог Джордж Кристофер Уильямс предположил, что некоторые гены в разном возрасте дают разный эффект: если в молодом возрасте они чрезвычайно важны для выживания, то в старости только вредят. Например, ген, увеличивающий фиксацию кальция в костях, снижает риск переломов в молодости, но увеличивает риск остеоартрита в старости из-за чрезмерной кальцификации суставов. Эта идея известна как антагонистическая плейотропия.
Укорочение теломер. Когда клетка делится, дочерняя цепь ДНК, образуемая на матрице родительской ДНК, становится несколько короче из-за особенностей работы фермента — ДНК-полимеразы. Дело в том, что ДНК-полимераза не может начать работу с нуля (соединить два свободных нуклеотида). Для нее на самом кончике ДНК специально создается РНК-затравка, к которой она начинает присоединять ДНК-нуклеотиды. Впоследствии РНК-затравка расщепляется, и генетическая информация о кончике хромосомы утрачивается. В череде клеточных делений концы хромосом становятся все более короткими и в определенный момент воспринимаются как повреждение ДНК, которое останавливает деление клетки.
Клетка с поврежденной ДНК в норме не делится, чтобы не переродиться в опухолевую. Это явление неспособности клетки с короткими теломерами делиться носит название клеточного старения. Поэтому на концах хромосом у млекопитающих расположены бессмысленные повторы, образующие теломеры, которые периодически достраиваются ферментом теломеразой. Однако теломераза после рождения выключается во всех клетках, кроме половых и некоторых стволовых. Поэтому с каждым делением клеток теломеры укорачиваются. К концу человеческой жизни они становятся настолько короткими, что каждое последующее деление ставит под угрозу генетическую информацию. Когда это происходит, прекращается деление, например, стволовых клеток и, как следствие, регенерация тканей.
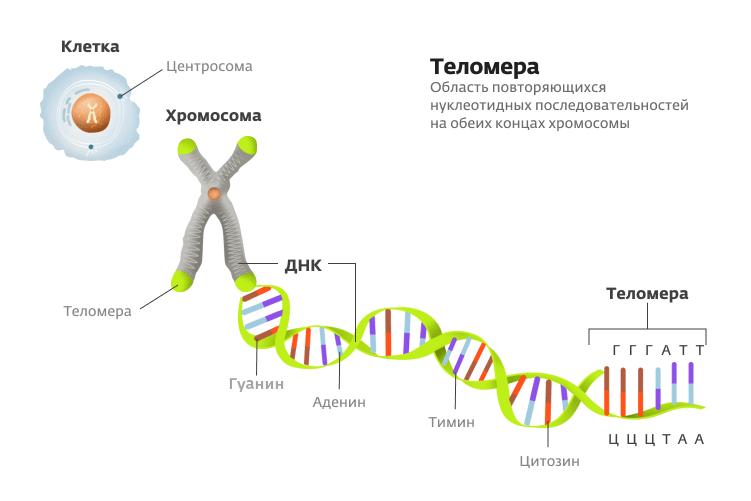
Теломера // Максим Мозуль
Цитоплазма — внутренняя полужидкая среда клетки, в которой расположены ядро и другие элементы мембранного и немембранного строения.
«Затухание» митохондрий. С возрастом утрачивают функцию «энергетические станции» клетки — митохондрии. Это происходит из-за накопления ошибок митохондриальных ДНК и ферментов, ослабления выбраковки поврежденных митохондрий. Перестает хватать энергии для процесса восстановления и роста, что тоже становится одной из причин старения. Кроме того, внутри клетки со временем нарушаются защитные барьеры. Митохондрии перегружаются кальцием и приоткрывают поры временной проницаемости. Через них в клетку выходят кольцевые митохондриальные ДНК, которые в цитоплазме клетки, где их в норме быть не должно, воспринимаются как инфекционное вторжение (некоторые вирусы и бактерии имеют подобные ДНК). Активируется интерфероновый ответ и хроническое воспаление, которое способствует развитию болезней.
Ухудшение качества белков. Со временем происходит нарушение круговорота внутриклеточных белков: поврежденные белки перестают заменяться новыми и накапливаются в организме. А внеклеточные белки, которые практически не обновляются, со временем образуют сшивки. Из-за них ткани становятся жесткими и неэластичными. Отсюда появление морщин, легочной недостаточности, повышенного артериального давления.
В неделящихся клетках (клетки сердечной мышцы, нейроны, которые не заменяются другими в течение почти всей жизни) постепенно скапливаются агрегаты (сгустки) белков, которые нарушают внутриклеточный трафик в цитоплазме, а некоторые из этих клеток довольно протяженные. Белки скапливаются и в эндоплазматической сети — внутренней транспортной и сортировочной системе клетки. Стресс эндоплазматической сети (это похоже на пробку на дороге), в свою очередь, запускает клеточное старение или гибель. Нередко сбиваются в агрегаты и белки вне клеток, бляшки амилоида и тяжи тау-белка в межклеточном пространстве головного мозга связывают с болезнью Альцгеймера — неизлечимой формой возрастной нейродегенерации.
Ослабление биологических барьеров. Ключевую роль для поддержания постоянства параметров внутренней среды играют биологические барьеры, которые находятся в кишечнике, стенке сосудов, коже, между головным мозгом и кровотоком. При старении эти барьеры нарушаются, и через них проникают инфекции, нежелательные молекулы или токсины. Это служит причиной разнообразных болезней: воспалений в стенке желудочно-кишечного тракта, атеросклероза и так далее.
Ночница Брандта — небольшая летучая мышь. Названа в честь немецкого зоолога Иоганна Брандта.
Борьба со старением
Хотя мы знаем о старении довольно много, этого недостаточно, чтобы эффективно и безопасно вмешиваться в эти процессы. Однако некоторые успешные эксперименты поставила сама природа. Так, полярная акула живет 400 лет. А голый землекоп почти не болеет раком, нечувствителен к боли и в неволе доживает до 30 лет, что необычайно долго для грызуна его размеров (13 см): лабораторная мышь живет около трех лет (10 см). По человеку довольно хорошо видно, сколько ему лет, чего не скажешь о голом землекопе: крайне тяжело определить по его внешнему виду, сколько он прожил. Считается, что долголетие землекопа обусловлено активным восстановлением поврежденных оснований ДНК. Более того, есть предположение, что голый землекоп является неотеническим животным — развитие его организма останавливается на стадии новорожденного. А самым удивительным долгожителем считается летучая мышь ночница Брандта: при массе тела всего в 5 грамм она доживает в дикой природе до 40 лет — обычно долго живут те звери, которые имеют наибольшую массу. Ученые расшифровывают геномы животных-долгожителей, что позволяет устанавливать новые генетические причины долголетия.

